华海药业冲击10亿美元品种 抗痛风药可在美销售
| 所在地区: | 广东-揭阳-试验区 | 发布日期: | 2022年4月2日 |
建设快讯正文
4月1日,华海药业公告称,公司向FDA申报的左乙拉西坦注射液、非布司他片的ANDA已获得批准,截至公告日,华海药业在上述两款产品已投入研发费用分别约598万元、1430万元。米内网数据显示,今年以来,华海药业获得FDA批准的ANDA已达5个。
左乙拉西坦注射液是由UCB研发的一款抗癫痫药,最早于2006年在美国上市,2021年优时比的左乙拉西坦全球销售额达9.7亿欧元(以4月1日汇率计,约10.7亿美元)。目前在美国境内,左乙拉西坦注射液的主要生产厂商包括Viatris、Aurobindo、Hikma等。
而在国内市场,华海药业于2020年11月以仿制4类提交左乙拉西坦注射用浓溶液上市申请,近日已步入行政审批阶段,有望于近期获批。
非布司他片是由Tekeda研发的一款黄嘌呤氧化酶抑制剂,主要用于痛风患者高尿酸血症的长期治疗。原研产品最早于2009年3月在美国上市,目前在美国境内,非布司他片的主要生产厂商有Viatris、Sun、Alembic等。
华海药业的非布司他片ANDA于2018年5月获得FDA暂时批准,此次为正式获得批准。而在国内市场,华海药业曾于2014年提交非布司他片上市申请,之后主动撤回,目前还处于开展BE试验阶段。
华海药业表示,左乙拉西坦注射液ANDA文号的获批及非布司他片获得正式批准,标志着公司具备了在美国市场销售上述产品的资格,这有利于公司不断扩大美国市场销售,强化产品供应链,丰富产品梯队,提升公司产品的市场竞争力,对公司的经营业绩产生积极的影响。
2022年至今华海药业获批的ANDA
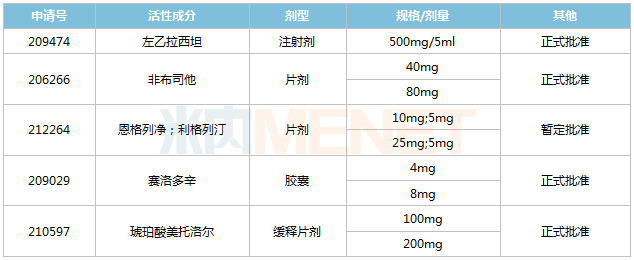
来源:米内网全球上市药物库
米内网数据显示,含左乙拉西坦、非布司他在内,今年以来华海药业已有5个ANDA获得FDA批准,其中恩格列净利格列汀为暂定批准。
来源:米内网数据库、上市公司公告等
注:数据统计截至4月1日,如有疏漏,欢迎指正!
按照客观、公正、公开的原则,本条信息受业主方委托独家指定在中国建设招标网 www.jszhaobiao.com 发布
注册会员 享受贴心服务
标讯查询服务
让您全面及时掌握全国各省市拟建、报批、立项、施工在建项目的项目信息。
帮您跟对合适的项目、找对准确的负责人、全面掌握各项目的业主单位、设计院、总包单位、施工企业的项目 经理、项目负责人的详细联系方式。
帮您第一时间获得全国项目业主、招标代理公司和政府采购中心发布的招标、中标项目信息。
标讯定制服务
根据您的关注重点定制项目,从海量项目中筛选出符合您要求和标准的工程并及时找出关键负责人和联系方式。
根据您的需要,向您指定的手机、电子邮箱及时反馈项目进展情况。
咨询热线:4000-156-001